L'approvisionnement en médicaments est en danger: le marché suisse perd de son attrait
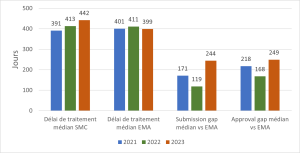 |
Demandes pour des nouvelles substances actives, toutes procédures (2021–2023) |
Basel (pts017/24.07.2024/15:00)
En Suisse, les patients-e-s accèdent de moins en moins facilement à des médicaments parfois vitaux. L'étude de benchmarking menée par Swissmedic et l'industrie a mis encore davantage en évidence le vrai problème auquel la Suisse est confrontée. En effet, le processus de l'OFSP visant à fixer le prix des médicaments et établir les modalités de leur prise en charge prend toujours plus de temps, et les conditions-cadres se péjorent, ce qui rend le marché suisse moins attrayant. Cette situation est problématique pour l'industrie pharmaceutique, et surtout pour les patient-e-s. Des solutions existent, mais au lieu de procéder à des réformes pourtant urgentes, la sphère politique aggrave la situation.
L'étude de benchmarking 2023 réalisée par l'industrie pharmaceutique et Swissmedic montre que la durée des processus d'autorisation de mise sur le marché a augmenté en Suisse, et que les entreprises soumettent leurs demandes plus tardivement. Par conséquent, en Suisse, un médicament est autorisé 249 jours (médiane calculée à partir de l'ensemble des processus) plus tard qu'auprès de l'Agence européenne des médicaments (EMA). Par ailleurs, une augmentation du retard de 48% est constatée par rapport à l'année précédente. Concrètement, en 2023, les entreprises ont déposé leur demande d'autorisation de mise sur le marché auprès de Swissmedic 244 jours (médiane calculée à partir de l'ensemble des procédures) après celle adressée à l'EMA. Cela ralentit encore davantage les processus. Les réglementations politiques actuelles sont en cause: la détérioration des conditions-cadres fait en sorte qu'on accorde de moins en moins la priorité au marché suisse. Cela nuit à l'industrie pharmaceutique, et surtout aux patient-e-s qui résident en Suisse.
René Buholzer, directeur d'Interpharma, déclare à ce sujet:
«Alors que les milieux politiques se focalisent entièrement sur les coûts, la sécurité de l'approvisionnement en pâtit, et les laboratoires pharmaceutiques qui ont des sites de recherche et de production sur notre territoire n'arrivent plus à planifier leurs opérations. La Confédération et le Parlement doivent revoir entièrement l'accès des patient-e-s aux médicaments innovants, afin d'éviter que l'industrie et l'approvisionnement en médicaments ne subissent des répercussions sur le long terme.»
Malheureusement, les résultats de l'étude WAIT (Patients W.A.I.T Indicator) de l'EFPIA confirment les effets néfastes de cette situation puisque, d'après ces données, seule la moitié des médicaments pris en charge en Allemagne sont également facilement accessibles aux patient-e-s suisses. Par ailleurs, selon des données d'Interpharma montrent que le délai d'attente pour accéder aux médicaments est désormais de 301 jours, depuis leur autorisation jusqu'à leur prise en charge par la caisse maladie.
(Ende)| Aussender: | Interpharma |
| Ansprechpartner: | Georg Därendinger |
| Tel.: | +41 61 264 34 00 |
| E-Mail: | georg.daerendinger@interpharma.ch |
| Website: | www.interpharma.ch |


